Introducing Adalimumab Biosimilar (ZRC-3197) for Inflammation Arthritis: Anti-TNF Therapies
MD
Faculty of Medicine Ramathibodi Hospital, Mahidol University

กลไกการทำงานของ TNF
TNF จับกับ TNF receptor จากนั้นจะเกิดการกระตุ้น signaling pathway โดยเฉพาะอย่างยิ่ง JAK ส่งผลให้มีการสร้างและปลดปล่อย pro-inflammatory cytokines (IL-1, IL-6 เป็นต้น) นอกจากนี้ TNF ยังช่วยให้แอนติเจนกระตุ้น T-cell โดยผ่าน antigen presenting cell ให้หลั่ง cytokine ต่างๆ และชักนำให้มีการหลั่งเอนไซม์หรือโปรตีนที่มาทำลายเนื้อเยื่อ เช่น matrix metalloproteinases และ prostanoids เป็นต้น นอกจากนี้ TNF ยังเพิ่มการแสดงออกของ adhesion molecules ทำให้ดึง inflammatory cells (T cells, neutrophils เป็นต้น) ที่มาอยู่บริเวณแผลมากขึ้น นอกจากนั้น TNF ยังกระตุ้น Macrophage หรือ Fibroblast ให้มีการปล่อยเอนไซม์ต่าง ๆ ออกมา ส่งผลให้เกิดการทำลายข้อหรือกระดูกเพิ่มขึ้น นอกจากนี้ ยังกระตุ้นกระบวนการ Osteoclastogenesis ทำให้มีการทำลายของกระดูก
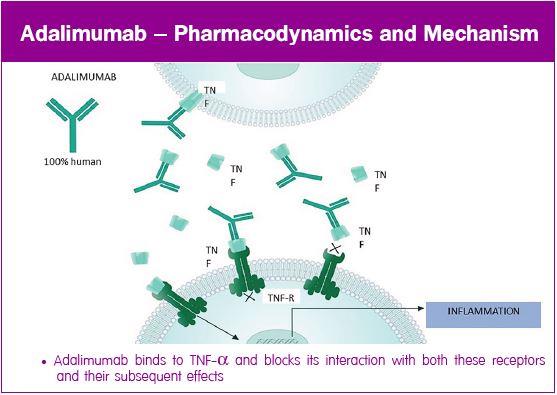
ยากลุ่ม Anti-TNF หรือ TNF inhibitors (TNFIs) แบ่งเป็น 2 กลุ่ม ได้แก่ กลุ่ม fusion proteins เช่น Etanercept ยากลุ่ม monoclonal antibody (mAb) ซึ่งแบ่งเป็น chimeric mAb ซึ่งโครงสร้างเป็นแอนติบอดีลูกผสมระหว่างของคนและหนู เช่น Infliximab และ กลุ่ม humanised mAb ได้แก่ Adalimumab, Golimumab และ Certilizumab pegol
Adalimumab เป็น humanised mAb ต่อ TNF โดยจับกับ TNF และซึ่งจะป้องกันไม่ให้ TNF ไปจับกับ TNF receptor ที่ผิวเซลล์ ส่งผลให้ยับยั้งการส่ง signal transduction เข้าไปในเซลล์ ดังนั้น การยับยั้งการจับกันของ TNF alpha ไม่ให้ไปจับกับ TNF receptor ส่งผลให้เกิดการยับยั้ง inflammation ที่จะเกิดขึ้นตามมาได้ Adalimumab มีข้อบ่งใช้ในโรคต่าง ๆ เช่น RA/JIA, AS, PA, Hidradenitis suppurative, Crohn’s disease/ulcerative colitis, Uveitis และเป็นยาที่มีประสบการณ์ใช้มากว่า 20 ปีทั่วโลก มีการศึกษามากกว่า 100 Global Cinical trials และ scientific publication มากกว่า 2,000 papers
Adalimumab biosimilar (ZRC-3197) ประกอบด้วยกรดอะมิโน 1,330 โมเลกุล มีน้ำหนักโมเลกุลประมาณ 148 Kda มีการศึกษาถึง Physicochemical and Functional Characterization1 และยังมีการศึกษา Randomized, Double-blind, Pararell group เปรียบเทียบ Adalimumab Biosimilar (ZRC-3197) กับ Originator ในผู้ป่วย RA
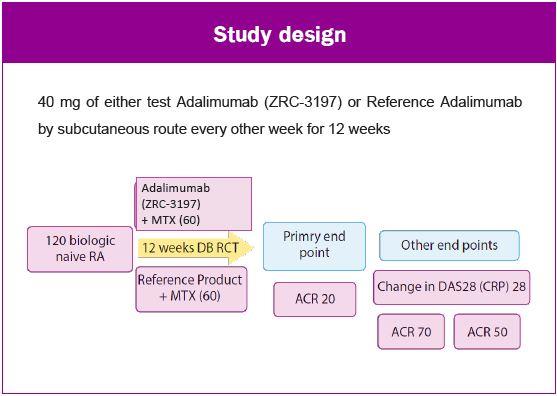
การศึกษานี้แบ่งคนไข้ RA 120 คน ที่ไม่เคยได้รับ biologic treatment มาก่อน เป็น 2 กลุ่ม กลุ่มละ 60 คน ให้ Adalimumab Biosimilar (ZRC-3197) 40 mg ฉีด sq ทุก 2 สัปดาห์ + Metrotrexate และอีกกลุ่มให้ Adalimumab originator 40 mg ฉีด sq ทุก 2 สัปดาห์ + Metrotrexate ติดตามไป 12 สัปดาห์ และดูผล primary end point คือ ACR20 และ Endpoints อื่น ๆ คือการเปลี่ยนแปลงของ DAS28-CRP, ACR50 และ ACR70 พบว่าผลที่ได้ในแง่ของ Efficacy, Safety และ Immunologenicity ของทั้ง 2 กลุ่มไม่มีความแตกต่างกัน ซึ่งผลของการศึกษานี้แสดงให้เห็นว่า Adalimumab Biosimilar (ZRC-3197) มี Biosimilarity ซึ่งเทียบในแง่ของ Efficacy, Tolerability และ Safety กับ Adalimumab originator ที่ไม่แตกต่างกัน ซึ่งทำให้ Adalimumab Biosimilar (ZRC-3197) ได้รับการรับรองจาก Regulation authority ในหลายประเทศ
นอกจากนี้ยังมีการศึกษา Retrospective study ใน Real life experience ของผู้ป่วย RA และ Spondyloarthropathy2 ที่ได้รับ Adalimumab biosimilar (ZRC-3197) ในผู้ป่วย RA จะดูค่า DAS28 และผู้ป่วย Sondyloarthropathy วัดที่ค่า BASDAI พบว่า DAS28 และผู้ป่วย BASDAI มีค่าลดลงอย่างต่อเนื่องเมื่อวัดที่เดือนที่ 3, 6, 12 เมื่อเทียบกับ baseline และผลยังคง maintain ต่อไปจนถึง 24 เดือน
การศึกษา “Adalimumab Biosimilar Patient Registry (ASPIRE)”3 ซึ่งเป็น post-marketing observational registry program มีศูนย์วิจัย 26 แห่ง เริ่ม Enrolled ผู้ป่วยในปี 2015 ติดตามในผู้ป่วย RA, AS, PsA และ JIA จำนวน 502 ราย ไปประมาณ 32-36 สัปดาห์ พบว่า ผู้ป่วยที่ได้รับ Adalimumab Biosimilar (ZRC-3197) มี Efficacy, Safety และ Tolerability ในระดับดีถึงดีมาก ช่วยลดความรุนแรงของโรค RA และ AS ลง ลด pain และ inflammatory marker ในในผู้ป่วย RA, AS, PsA และ JIA
นอกจากนี้ในเรื่องของ Safety ยังมีการศึกษา “Real-life Safety Profile of ZRC3197 (Adalimumab Biosimilar) in Indian Patients with Common Rheumatic Diseases” 4 เป็น Retrospective study ทำการติดตามเก็บข้อมูลความปลอดภัยจากผู้ป่วย rheumatic diseases ที่ได้รับ Adalimumab biosimilar (ZRC-3197) ผลการศึกษา พบว่า ไม่มีการค้นพบหลักฐานใหม่ของ AEs มีการเกิด Injection site reaction เพียง 1 ราย เนื่องจาก Adalimumab biosimilar (ZRC-3197) ใช้ Succinate buffer ในสูตรผสม จึงช่วยให้ลดอาการปวดบริเวณที่ฉีดยาลงได้ โดยจะแตกต่างกับ Adalimumab originator ที่ใช้ Citrate buffer อีกทั้ง Adalimumab biosimilar (ZRC-3197) ยังมีระบบ PreventisTM technology ที่ออกแบบเพื่อจะป้องกัน needle stick injuries อีกด้วย
โดยสรุป Adalimumab biosimilar (ZRC-3197) เป็น The World First Biosimilar ของ Adalimumab ที่มี Biosimilarity ที่ดี และมีการศึกษาที่เปรียบเทียบ Efficacy, Safety, Torelability และ Immunogenicity ที่ไม่แตกต่างจาก Adalimumab Originator ทั้งยังมี Succinate buffer ที่ช่วยลดอาการปวดบริเวณที่ฉีด และเข็มที่มี PreventisTM technology ที่จะป้องกัน needle stick injuries ดังนั้น Adalimumab biosimilar (ZRC-3197) จึงเป็นอีกทางเลือกหนึ่งในการเลือกใช้ยา Biosimilar สำหรับผู้ป่วย Inflammatory Arthritis ในประเทศไทย